영국 바이오뱅크(Biobank)의 혈장 단백질 level과 희귀 변이의 연관성 분석
Abstract
인간의 유전체와 단백체를 통합 분석하면 질병 메커니즘을 밝히는 데 도움이 되며, 임상 바이오마커를 식별하고 약물 표적을 발견하는 데에도 유용합니다. 이전의 프로테오게놈 연구는 주로 genome-wide association studies를 통한 흔한 변이(common variants) 에 중점을 두었고 혈장 단백체에 대한 희귀 변이(rare variants)의 기여는 잘 알려져 있지 않았습니다.
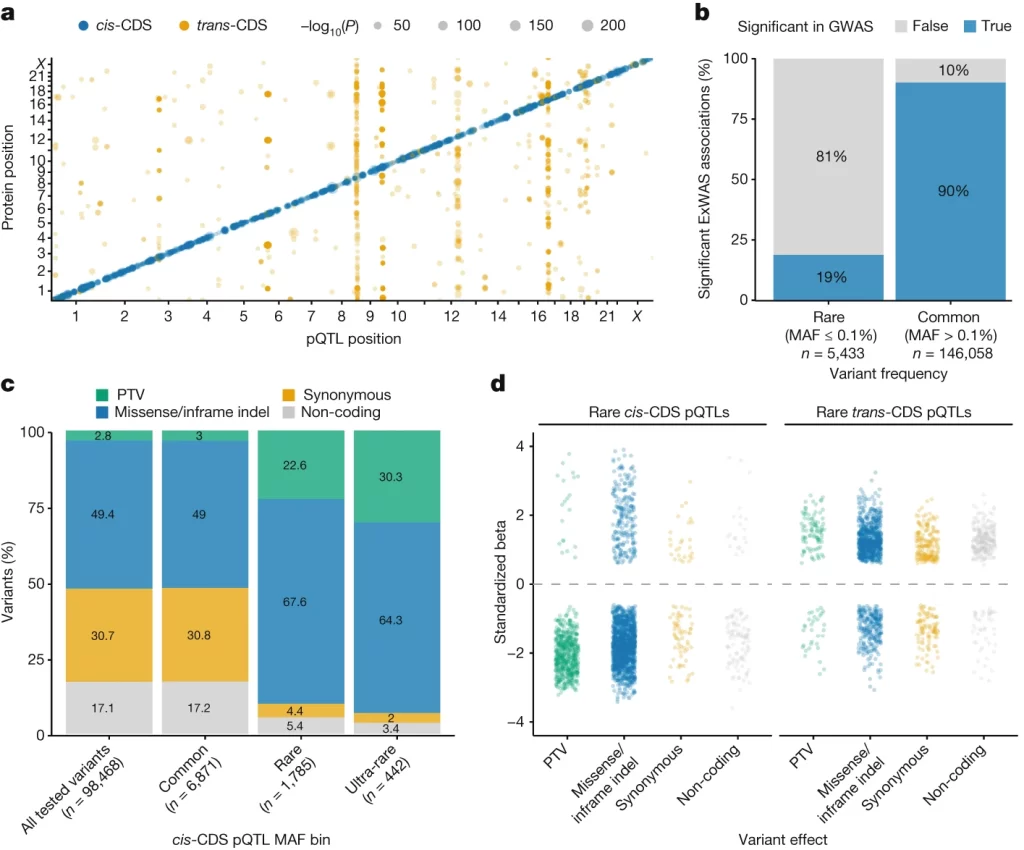
우리는 49,736명의 UK Biobank 참가자에서 측정된 2,923개의 혈장 단백질과 단백질을 코딩하는 희귀 변이 간의 관계(variant level association)를 확인했습니다. 우리의 연구에서는 5,433개의 희귀한 유전자 변이와 단백질 간의 관계를 발견했고, 이 중 81%는 이전 연구에서는 발견되지 않았습니다.다음으로 우리는 유전자 수준(gene level)의 통합 분석을 사용하여 유전자 수준에서 합쳐진 신호들을 살펴봤습니다. 이로 인해 1,962개의 유전자-단백질 관계가 드러났습니다. 단백질 절단 변이로부터 비롯된 691개의 유전자 수준 신호 중 99.4%가 감소된 단백질 발현과 연관되어 있었습니다. STAB1과 STAB2는 혈장 단백질 제거에 관여하는 스캐벤저 수용체를 인코딩하며, 각각 77개와 41개의 단백질 연관성을 가진 다발성(pleiotropic) loci로 나타났습니다. 우리는 여러 응용 사례를 통해 공개적으로 접근 가능한 자원(UK biobank를 의미)의 유용성을 보여줍니다. 사례로는 NLRC4의 대립 유전자 시리즈(allelic series)의 상세화, 지방간 질환과 관련된 변이인 HSD17B13에 대한 잠재적인 바이오마커 식별, 절단 단백질변이를 통합한 pQTL 분석을 통해 phenome-wide association studies를 강화가 있습니다.마지막으로 우리는 클로날 혈소판형성(CH:clonal haematopoiesis)의 proteomic consequences를 발견하였습니다. 유전자 변이인 TET2-CH와의 연관성과 FLT3의 단백질 발현이 증가하는 것을 확인하였습니다.
우리의 연구는 혈장 단백질의 발현량에 희귀 변이의 중요한 역할을 보여주었고 새로운 치료를 발견하는데 있어서 프로테오게놈학의 가치를 강조합니다.