mTOR-regulated mitochondria 대사 작용은 mycobacterium에 의한 세포 독성을 감소시킨다
Abstract
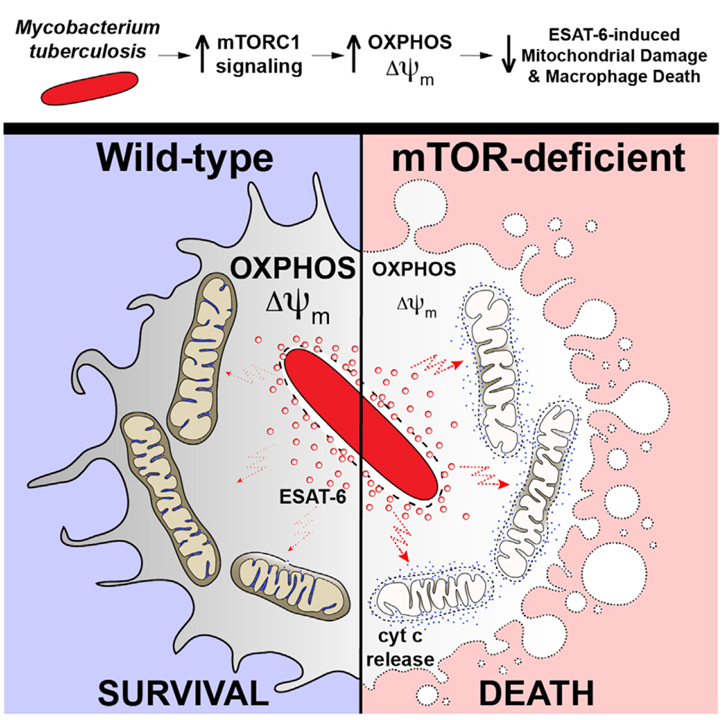
결핵의 특징적인 면역학적 구조인 granuloma에서 macrophage의 necrosis는 숙주에 대한 감수성을 증가시키는 주요한 pathogenic event입니다. Zebrafish의 forward genetic screening을 통해 우리는 대사 작용의 master regulator인 mTOR kinase를 결핵의 초기 숙주 저항 인자로 확인했습니다. 우리는 mTOR complex 1이 mycobacterium 감염에 의해 증가되는 glycolysis에 의한 mitochondrial energy metabolism으로 유도되는 cell death로부터 macrophage를 보호하는 것을 확인했습니다. 이러한 metabolic adaptation은 분비된 mycobacterial virulence determinant인 ESAT-6으로 인한 mitochondria 손상과 cell death를 예방하는데 필요합니다. 따라서 숙주는 에너지 대사를 조절함으로써 초기의 중요한 mycobacterial virulence mechanism에 효과적으로 대응할 수 있습니다. 그를 통해 pathogen-specific immune mechanism이 진행될 시간을 벌 수 있습니다. 우리의 연구 결과는 Mycobacterium tuberculosis가 인류에게 가장 치명적인 병원균임에도 불구하고 소수의 감염자에게만 작용하는 이유를 설명할 수 있습니다.
Figures
Fig 1. mTORC1-deficient zebrafish는 Mm 감염에 대해 과민 반응을 보입니다.
(A) Hindbrain ventricle (hbv) 및 caudal vein (cv) 주입 경로.
(B) 감염 4일 후(day post-infection : dpi) mtorfh178/fh178 또는 WT sibling (mtor+/+)에 대한 widefield mycobacterial fluorescence (Mm, 빨간색)과 bright field를 중첩시킨 현미경 사진.
(C) mtorfh178/+ incross 4dpi의 동물에서 bacterial fluorescence (fluorescent pixel count : FPC)의 정량화 그래프.
(D) 4dpi의 mtorfh178/fh178 와 Tg(mpeg1:YFP)를 발현하는 WT sibling의 공초점 현미경 사진.
(E-J) 4dpi의 동물의 mycobacterial cording 결과. 각각 다음과 같은 형질을 가진다. (E) mtorfh178/+ incross, (F) mtorsa16755/+ incross, (G) mtorfh178/+ x mtorsa16755/+ cross, (H) rptorsa11537/+ incross, (I) rictorasa15967/+; rictorbsa18403/+ double heterozygote incross, (J) torin1 (400nM), rapamycin (400nM), 0.5% DMSO (vehicle control)로 처리된 WT 5dpi 동물.
Fig 2. mTOR의 결핍은 macrophage 발달과 생존을 손상시키고 감염된 macrophage를 mycobacterium-induced cytotoxicity에 민감하게 만듭니다.
(A) Rapamycin 또는 DMSO를 처리한 Tg(mfap4:tdTomato-CAAX) zebrafish에서 granuloma의 연속 공초점 현미경 사진.
(B) (상단) Macrophage 계수 영역 (밝은 파란색 영역). (하단) Tg(mpeg1:tdTomato)를 발현하는 Mm-과 mock-으로 감염된 Raptor 돌연변이와 그 sibling의 macrophage 수.
(C) (상단) Rapamycin 및 DMSO 처리 기간. (하단) 5dpi의 mycobacterial cording.
(D) mtorsa16755/sa16755에서 죽어가고 있는 감염된 macrophage의 시간 경과 공초점 현미경 사진.
(E–G) 2dpi에서 mtorfh178/fh178 와 Tg(mpeg1:YFP)를 발현하는 mTOR-sufficient sibling의 6시간 시간 경과 공초점 현미경 이미지.
(E) 필드 당 감염된 macrophage의 수.
(F) 필드 당 죽어가는 감염된 macrophage의 백분율.
(G) mtor-/- 및 mTOR-sufficient fish의 죽어가는 macrophage에서 상대적인 mycobacterial burden.
(H) 4dpi embryo에서 WT Tg(mpeg1:tdTomato) 및 mtorfh178/fh178로 구성된 parabiotic zebrafish의 광시야 현미경 사진.
(I) 4dpi의 WT-mtor-/- parabiont에서 WT body (상단)와 mtor-/- body (하단)에서 macrophage의 수.
(J) 4dpi의 WT-mtor-/- parabiont에서 WT body (상단)와 mtor-/- body (하단)에서 감염의 최대 강도 예측 결과.
(K) 4dpi에서 WT Tg(mpeg1:tdTomato) 및 mtorfh178/+; Tg(mpeg1:YFP) parabiont의 광시야 현미경 사진
(L) WT-mtor+/- parabiont에서 WT body (상단)와 mtor+/- body (하단)에서 macrophage의 수.
(M) 4dpi의 WT-mtor+/- parabiont에서 WT body (상단)와 mtor+/- body (하단)에서 감염의 최대 강도 예측 결과.
Fig 3. mTOR 결핍은 macrophage에서 basal and mycobacterium-stimulated mitochondrial metabolism을 손상시킵니다.
(A) 감염된 동물에서 mROS 검출을 보여주는 공초점 현미경 사진.
(B) MitoTracker Red CMH2-Xros는 1dpi에서 mtor-/- 동물과 그 sibling의 감염 및 비감염 macrophage의 mean fluorescence intensity (MFI).
(C-K) THP-1 macrophage에 torin1 또는 DMSO를 처리하고 (C, D, G, H-K) tdTomato- 또는 (E, F) mWasabi-expressing Mm으로 multiplicity of infection (MOI)
(C) 2dpi에서 cell viability에 대한 flow cytometry plot.
(D) Non-viable cell의 정량화 결과.
(E) 1dpi에서 TMRE fluorescence에 대한 flow cytometry histogram.
(F) 1dpi에서 TMRE geometric mean fluorescence intensity (GeoMFI).
(G) 1dpi THP-1 macrophage 106만큼 있는 well당 ATP 농도.
(H–K) tdTomato-expressingMm (MOI=2)으로 감염된 1dpi THP-1 macrophage culture를 serum-free media에서 진행했고 torin1 또는 DMSO로 4시간 동안 처리했습니다.
(I, K) 감염되지 않은 세포와 감염된 세포에서 (I) phospho-S6S235/S236, (K) total S6 staining의 평균 형광 강도 (MFI).
Fig 4. mTOR 결핍은 mycobacterium-induced, mitochondrially mediated cell death를 촉진합니다.
(A, B) THP-1 macrophage는 MOI=3에서 (A, B) tdTomato 또는 (C, D) BFP-expressing Mm으로 감염되었습니다.
(A) Infected viable cells (FVD eFluor 660) 감염 후 7시간 (hour post-infection : hpi)에서 cytochrome c (cyt c) 형광에 대한 flow cytometry histogram.
(B) 7hpi Cyt clow 세포에서의 정량화 결과.
(C, D) Torin1을 처리한 THP-1 macrophage는 32hpi에서 Sytox Green으로 imaging하기 전에 TMRE와 MitoTracker Deep Red로 표지되었습니다.
(C) 감염되지 않은 macrophage에 둘러싸여 죽어가는 감염된 macrophage의 공초점 현미경 사진.
(D) 시간이 지남에 따라 죽어가는 감염된 macrophage의 TMRE, MitoTracker Deep Red, Sytox Green staining의 MFI.
Fig 5. Glycolysis 억제는 mitochondrial metabolism을 손상시키고 감염된 macrophage를 mycobacterium-induced cytotoxicity에 민감하게 만듭니다.
(A-C) Torin1 (400nM), 2-deoxy-D-glucose (2DG, 5mM), DMSO를 처리한 THP-1 macrophage는 각각 다음을 발현하는 Mm에 감염되었습니다. (A) BFP2, (B) tdTomato 또는 (C) tdTomato를 발현하는 Mtb.
(A) 1dpi에서 TMRE GeoMFI.
(B, C) 1dpi에서 non-viable cell의 백분율 (FVD eFluor 660+)
(D–I) Zebrafish는 caudal vein을 통해 ~150 fluorescent Mm으로 감염되었습니다.
(D) 50mM 2DG 또는 0.5% DMSO를 처리한 mock- 또는 Mm- 에 감염된 Tg(mpeg1:YFP) zebrafish의 몸에 있는 5dpi macrophage 수.
(E, F) Tg(mpeg1:YFP) 3dpi의 6시간 경과 공초점 현미경 이미지.
(G) 2DG 또는 DMSO를 5dpi 처리한 WT 동물의 cording.
(H) UK5099 (10μM) 또는 0.5% DMSO를 5dpi로 처리한 WT 동물의 cording.
(I) ndufaf1 G0 crispant와 WT sibling의 5dpi cording.
Fig 6. mTOR, glycolysis, OXPHOS의 결핍은 macrophage를 mycobacterial ESAT-6 dependent cytotoxicity에 민감하게 만듭니다.
(A) MOI=3으로 BFP2-expressing WT 또는 ΔESX-1 Mm에 감염된 7hpi의 THP-1 macrophage에서 Cytochrome c를 방출합니다.
(B) MOI=1에서 tdTomato-expressing WT 또는 ΔESX-1 Mm을 사용하여 감염시켰을 때 1dpi에서 4시간 경과 동안 죽어가는 세포 (Sytox Green+)의 백분율.
(C-J) Zebrafish는 caudal vein을 통해 해당 strain의 tdTomato-expressing Mm의 용량 일치 접종 방식으로 감염되었습니다.
(C) mtorfh178/fh178 및 Tg(mpeg1: YFP)를 발현하는 mtor-sufficient sibling의 2dpi 시점에서 intramacrophage의 Mm burden을 확인하는 6시간 시간 경과 공초점 현미경 이미지.
(D) (C)와 동일한 실험에서 죽어가는 감염된 macrophage의 백분율.
(E) mtorfh178/fh178 동물 및 mtor-sufficient sibling의 4dpi에서의 cording.
(F, G) 2DG, UK5099 또는 DMSO를 5dpi로 처리한 WT zebrafish의 cording.
(H) ndufaf1 G0 crispant와 WT sibling의 5dpi에서의 cording.
(I) mtorsa16755/sa16755 동물 및 mtor-sufficient sibling의 4dpi에서의 cording.
(J) mtorfh178/fh178 동물 및 ΔesxA Mm의 4dpi에서의 cording.
Fig 7. ESAT-6은 phagosomal permeabilization에 관여하는 downstream mTOR-deficient macrophage에서 mitochondria 손상을 매개합니다.
(A-E) Torin1 및 DMSO 처리 THP-1 macrophage를 MOI=3에서 tdTomato-expressing WT 또는 ΔESX-1 Mm으로 감염시키고 7시간 동안 prazosin (PRZ, 20μM)으로 처리했습니다.
(A) THP-1 macrophage 7hpi에서 galectin-8 (GAL8) immunofluorescence와 Mm fluorescence의 공초점 현미경 사진.
(B) GAL8-associated Mm foci가 있는 macrophage의 백분율.
(C) 7hpi에서 GAL8 foci 관련된 Mm volume의 백분율.
(D) 7hpi에서 Cytochrome c를 방출한 세포의 백분율.
(E) mtorsa16755/sa16755 물고기와 mtor-sufficient sibling은 2dpf (days post-fertilization)에서 hindbrain ventricle을 통해 ~90 fluorescent Mm으로 감염 후 cording 결과.
(F) 400nM rapamycin을 처리한 WT fish는 2dpf의 hbv를 통해 WT 또는 point mutant Mtb esxA로 보완된 ~180 tdTomato-expressing ΔesxA Mm으로 감염 후 cording 결과.