천연물 유래 sequanamycin의 강력한 경구용 항-결핵제 발굴
Abstract
약제 내성 결핵의 출현으로 새로운 항-결핵제가 절실히 필요하게 되었습니다. 이 연구에서는 Mycobacterium tuberculosis (Mtb)에 대해 뛰어난 시험관 내 및 생체 내 활성을 가진 sequanamycins라고 하는 일련의 macrolides의 발견을 보고합니다.
Sequanamycin은 erythromycin 및 clarithromycin과 같은 고전적인 macrolides와 유사한 방식으로 리보솜과 상호작용하는 세균성 리보솜 억제제이지만, Mtb의 고유한 macrolides 내성을 극복할 수 있는 결합 특성을 가지고 있습니다. 결합된 억제제가 있는 리보솜의 구조는 진보된 리드 화합물 SEQ-9를 생산하기 위해 sequanamycin을 최적화하는 데 사용되었습니다. SEQ-9는 급성 및 만성 TB의 마우스 모델에서 단일 작용제로서 효능이 있었고, 다른 TB 약물과 함께 뮤린 TB 감염 모델에서 살균 활성을 입증했습니다.
이러한 결과는 약물 감수성 및 약물 내성 결핵에 대한 새로운 요법에 사용할 가능성이 있는 결핵 임상 후보로서 이 시리즈의 추가 연구 근거가 됩니다.
Figure
[Figure 1] Sequanamycin과 T. thermophilus 리보솜의 주요 상호작용
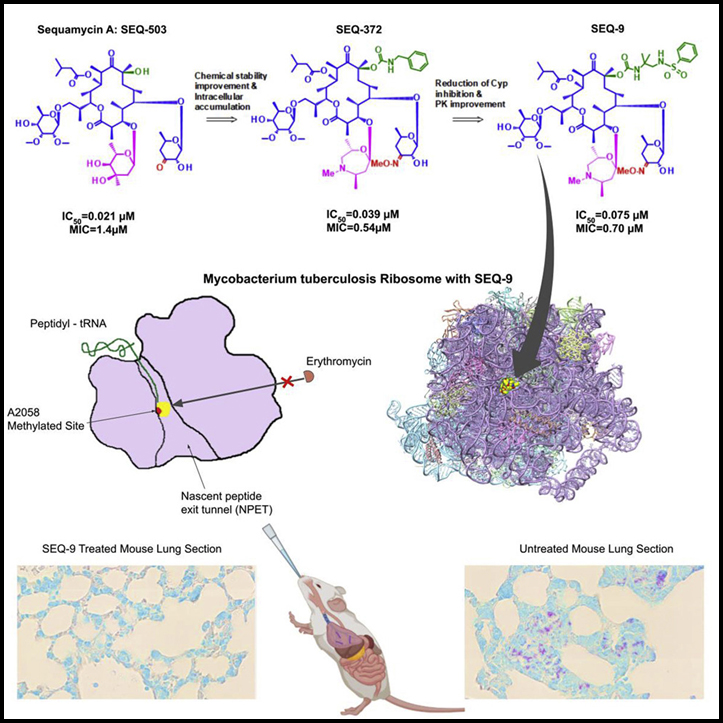
(A) Erythromycin, sequanamycin A와 그 유도체의 구조.
(B) SEQ-977, SEQ-569의 2D 상호 작용 다이어그램.
(C) SEQ-977의 맞춤 (파란색) 및 펩티드 출구 터널의 벽 (노란색과 흰색) 사이에 형성된 상호작용.
(D) SEQ-977의 C13에서 mycinose와 23S rRNA의 L22 및 도메인 II의 터널 벽 요소에 의해 형성된 상호작용.
(E) SEQ-569 (노란색) 및 SEQ-977 (보라색)에 대한 C8에서 carbamate 존재 하의 A2062의 상대 위치.
[Figure 2] SEQ-977의 C13 mycinose에 인접한 헬릭스 35에서 G741과 G743의 위치
G741과 G743의 제거는 나선의 구조를 변경하여 mycinose 그룹과 나선 및 L22 Arg90의 상호 작용 방해.
[Figure 3] A2058과 함께 C5에서 ketoallose의 위치 및 상호작용
(A) Mtb에 결합된 SEQ-9 (노란색)의 cryo-EM 구조와 함께 T. thermophilus에서 SEQ-977 (회색) 및 erythromycin (보라색, PDB: 6XHX 및 파란색, PDB: 4V7X)의 위치 리보솜.
(B) 각각의 macrolides의 3′-hydroxyl group과 A2058의 N1기 사이에 형성된 수소 결합.
(C) 3개의 macrolides 및 각각의 A2058 잔기의 ketoallose 그룹의 중첩 및 상이한 보기.
(D) SEQ-977의 중성 sp2 수소화 옥심과 비교하여 erythromycin (6XHX)의 하전된 sp3 수소화 dimethylamine.
[Figure 4] SEQ-9와 Mtb 리보솜의 주요 상호작용
(A) SEQ-9의 2D 상호작용 다이어그램.
(B) T. thermophilus에서 형성된 상호작용과 다른 Mtb 리보솜의 mycinose C13 및 G748에 의해 형성된 상호작용.
[Figure 5] SEQ-9 처리 후 Mtb 감염 BALB/c 마우스의 폐에서 SEQ-9의 생체 내 활성
(A) 급성 TB 마우스 모델에서 SEQ-9 용량 범위.
(B) 만성 TB의 마우스 모델에서 SEQ-9 용량 범위.
(C) TB의 단기 (고도) 급성 마우스 모델에서 SEQ-9 용량 범위.
[Figure 6] TB의 마우스 모델에서 치료의 집중 단계 동안 항-결핵 약물과 함께 투여된 SEQ-9
각 약물 용량
SEQ-9 300mg/kg/day
Bedaquiline (B) 25mg/kg/day
Pretomanid (Pa) 100mg/kg/day
Linezolid (L) 100mg/kg/day
Pyrazinamide (Z) 150mg/kg/day.
Disscussion
Sequanamycin A는 1960년대 잠재적인 결핵 치료제로 상당한 관심을 받았지만 완전히 개발된 적은 없는 자연 발생 macrolides입니다. 새로운 항생제에 대한 현재의 필요성으로 인해 Mtb 특이적 제제로서 이 화합물에 대한 관심이 되살아났습니다. Sequanamycin은 나머지 erythromycin 계열 macrolide와 달리 Mtb에 대해 강력한 활성을 나타낸다는 점에서 macrolide 중에서 독특합니다. Clarithromycin과 마찬가지로 이들은 ribosomal peptide 출구 터널과 상호 작용하지만 나머지 erythromycin 계열 macrolides와 비교하여 sequanamycins의 다양한 효능을 설명하기에 충분한 구조적 차이가 있습니다. 실제로, erm37에 의한 메틸화는 다른 macrolide와 일치하는 sequanamycin 처리에 의해 유도되지만, sequanamycin에 의한 억제에는 영향을 미치지 않습니다. 왜냐하면 이들은 천연 및 메틸화된 Mtb 리보솜에 대해 동일한 억제 활성을 보이기 때문입니다. SEQ-9를 갖는 Mtb 리보솜의 cryo-EM 구조는 메틸화 리보솜에 대항하여 효능을 유지하는 sequanamycin의 능력에 대한 분자적 기초가 일반적으로 모든 macrolide 항생제에서 발견되는 desosamine의 dimethyl 그룹과 입체적 중첩을 갖는 A2058의 메틸화 N6의 약간의 재배치에 기인한다는 것을 명확하게 보여줍니다. Sequanamycins에는 부피가 큰 dimethyl 그룹이 없으며 A2058의 N6의 약간 다른 위치와 결합되어 sequanamycin macrolide가 상당한 친화력 손실 없이 주머니에 결합할 수 있습니다.
SEQ-569 및 SEQ-977과 함께 T. thermophilus 리보솜의 공결정 구조를 사용하여 효능뿐만 아니라 ADME 특성도 향상시키는 변형을 합리화했습니다. 이러한 최적화는 대식세포 내부에 존재하는 복제 및 비복제 Mtb, Mtb 및 다수의 임상 분리주에 대한 실험실 변종에 대해 강력한 시험관 내 활성을 입증한 SEQ-9로 이어졌습니다.
SEQ-9는 새로운 항-결핵 약물의 중요한 특징인 개별 1차 또는 2차 약물에 대한 Mtb 내성에도 효과적이었습니다. 생쥐의 PK와 함께 SEQ-9의 약리학적 활성은 그것이 폐 조직에 잘 분포하고 1일 1회 경구 투여에 매우 적합할 수 있음을 보여줍니다. 급성 및 만성 감염 마우스 모델에서 이 화합물은 단일 제제 및 linezolid, bedaquiline, pretomanid, pyrazinamide와 조합하여 생체 내 효능을 입증했습니다. SEQ-9가 TB의 마우스 모델에서 테스트된 모든 TB 약물에 대해 부가적 활성을 보인 것은 주목할 만하며, 이는 이러한 종류의 macrolides가 광범위한 TB 약물 및 요법에 기여할 가능성이 있음을 시사합니다. SEQ-9를 bedaquiline, pretomanid와 조합할 때 4주와 8주 사이에 살균 효과의 현저한 가속이 입증되었습니다. 치료 8주 후, bedaquiline/pretomanid/SEQ-9의 3개 약물 조합은 평균 로그 CFU 수를 0.2로 감소시켰고, 이는 SEQ-9 부재 시 bedaquiline/pretomanid의 경우 1.69 (p < 0.01)에 비해 감소했습니다. 치료 마지막 4주 동안 bedaquiline/pretomanid에 실질적인 살균 활성을 추가하는 SEQ-9의 능력. 동일한 마우스 모델에 대한 이전 연구에서는 linezolid가 bedaquiline/pretomanid에 유사한 기여를 함을 보여주었으며, 그 결과 Nix-에서 XDR-TB 치료에서 6개월 경구 요법으로 우수한 치료 결과를 생성한 3제 BPaL 요법이 나타났습니다. 이것은 sequanamycin 시리즈가 Mtb 리보솜을 표적으로 하는 치료 무기를 풍부하게 할 수 있는 linezolid의 잠재적 대안으로 추가로 탐구되어야함을 시사합니다.