Aspirin prevents metastasis by limiting platelet TXA2 suppression of T cell immunity
아스피린은 혈소판 TXA2가 T세포 면역을 억제하는 것을 제한함으로써 전이를 억제한다. Abstract 전이는 암세포가 원발 종양에서 먼 장기로 퍼지는 현상이며, 전 세계적으로 암 사망의 90%를 차지하는 주요 원인이다. 전이되는 암세포는 기존의…
아스피린은 혈소판 TXA2가 T세포 면역을 억제하는 것을 제한함으로써 전이를 억제한다. Abstract 전이는 암세포가 원발 종양에서 먼 장기로 퍼지는 현상이며, 전 세계적으로 암 사망의 90%를 차지하는 주요 원인이다. 전이되는 암세포는 기존의…
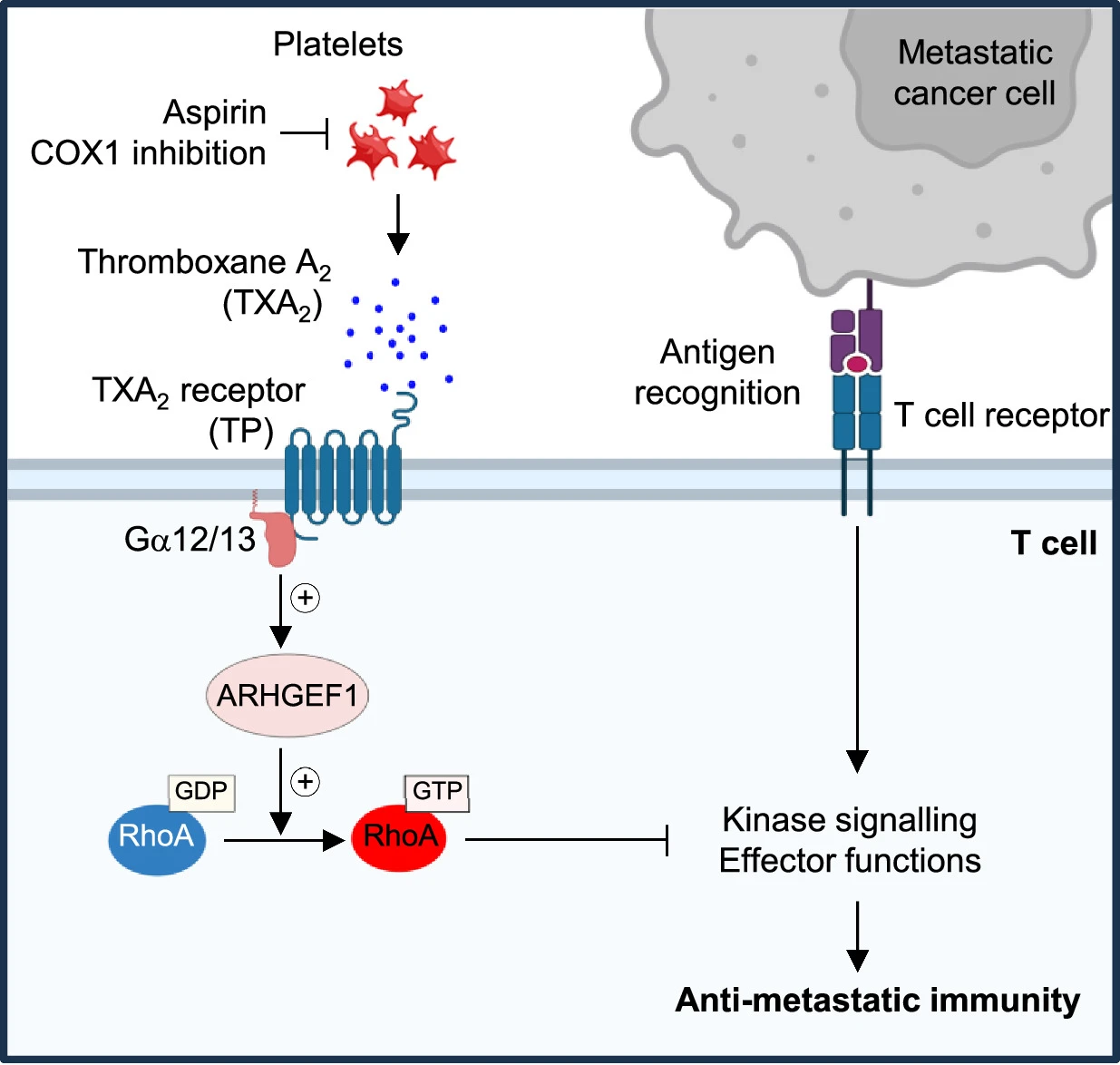
아스피린은 T 세포 면역을 억제하는 혈소판 TXA2 제한을 통해 전이를 방지한다 Abstract 전이는 암세포가 원발성 종양에서 멀리 떨어진 장기로 퍼지는 현상으로, 전 세계적으로 암 사망의 90%의 원인이 된다. 전이하는 암세포는…
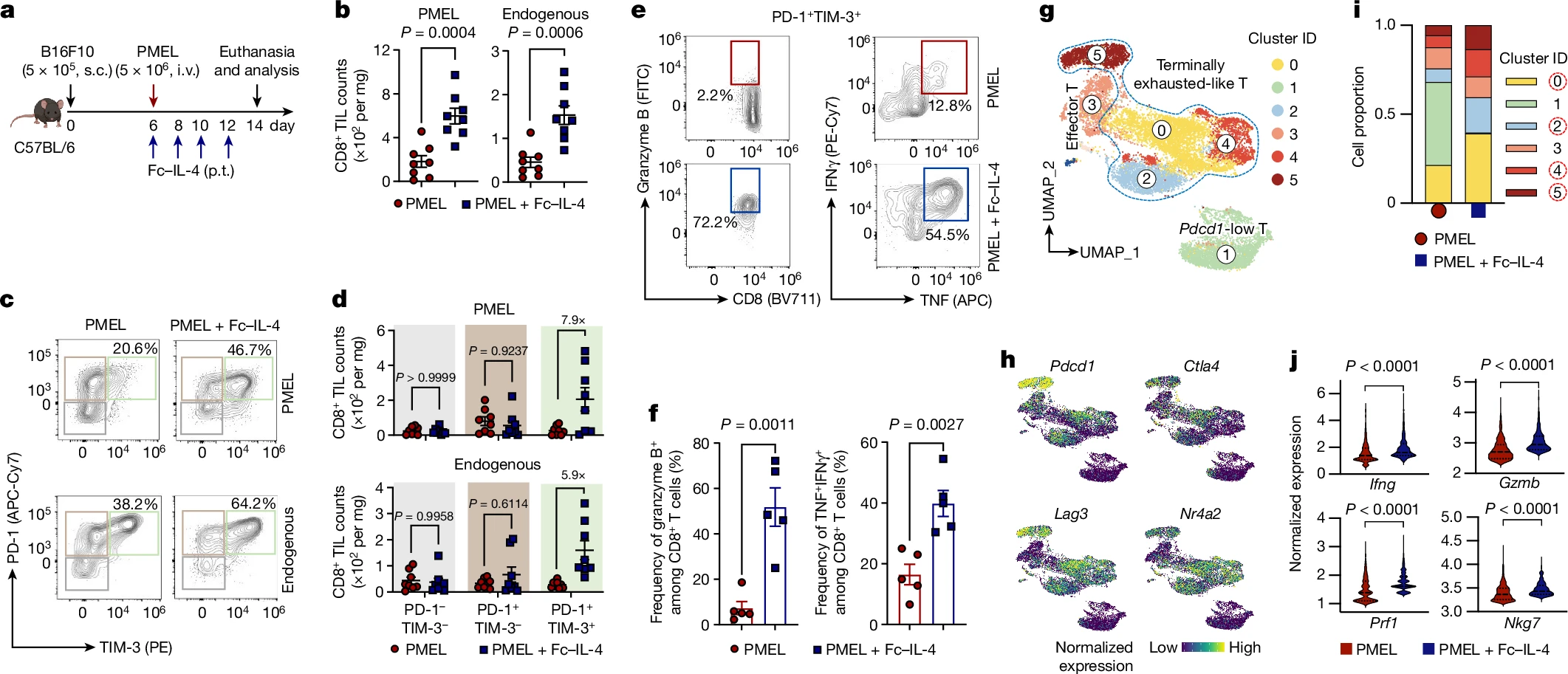
type 2 cytokine Fc-IL-4는 exhausted CD8+ T cell을 활성화하여 암에 대항한다 Abstract 현재의 암 면역 요법은 주로 암과 싸우는 type 1 면역 반응을 유도하는 데 중점을 두고 있지만, 장기적인 완전…
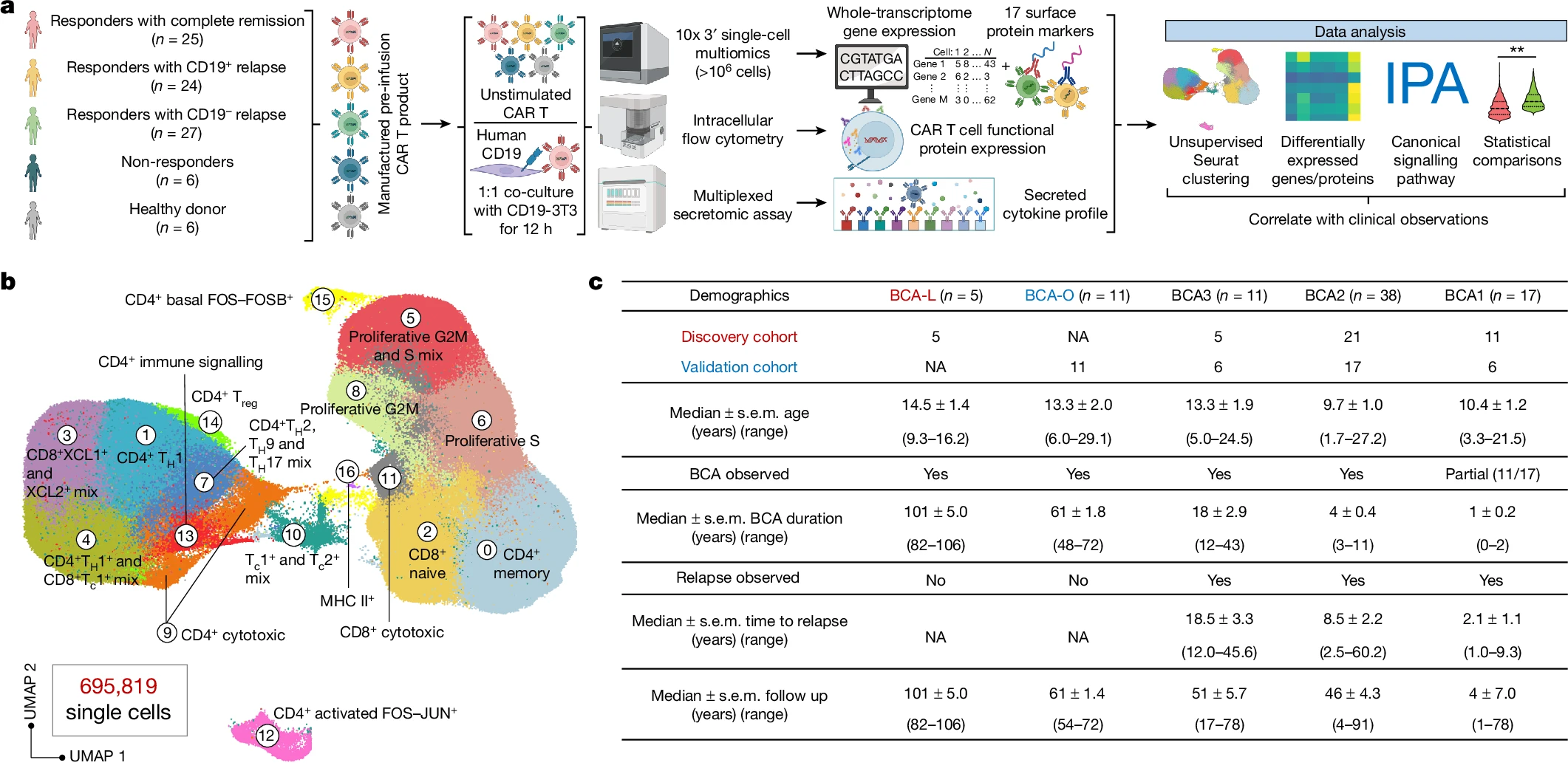
Single-cell CAR T 아틀라스가 8-year leukaemia remission에서 type 2 function을 밝혀낸다 Abstract Acute lymphocytic leukaemia(ALL)에 대한 chimeric antigen receptor (CAR) T cell 치료의 높은 반응률에도 불구하고 약 50%의 환자가 첫해…
ILC2 유래 LIF licence는 조직에서 전신 면역으로 진행됩니다 Abstract 면역 세포의 이동과 정착은 면역 감시에서 중요한 역할을 합니다. 이 과정은 면역 세포가 화학주성 신호에 반응하여 조직과 림프계 내의 특정 위치로…
인체 SARS-CoV-2 감염 모델을 통해 국소 및 전신 면역 반응 역학을 밝히다 Abstract COVID-19 팬데믹은 여전히 지속 중이며 위협적이지만, 이 질병에 대한 초기 세포 반응의 역학에 대한 이해는 제한적입니다. 이…
면역 미세 환경이 장 내 Treg 기능을 조절한다. Abstract 장의 면역 시스템은 공생 미생물과 자가 항원에 대한 내성을 유지하면서 침입하는 병원체로부터 방어할 수 있도록 매우 적응되어 있다. 장의 복잡한 면역…
CARD8 염증체는 HIV/SIV 병인학과 질병 진행에 지배적인 역할을 합니다. Abstract CD4+ T 세포 감소는 HIV에 감염된 사람들과 SIV-infected macaques는 SIV(Simian Immunodeficiency Virus)에 감염된 원숭이에서 질병 진행의 주요 원인이지만, 대부분의 감염되지 않은…
IL-10은 sphingolipid metabolism 억하여 염증을 제한합니다. Abstract Interleukin-10(IL-10)은 innate immune cell types에서 immune cell activation과 사이토카인 생산을 제한할 수 있는 주요 anti-inflammatory cytokine입니다. IL-10 신호가 손실되면 사람과 mice에서 생명을 위협하는…