Tip cell 전문화에 의한 Brain-speciric 혈관형성 메커니즘
Abstract
척추동물의 장기는 지역적으로 적응된 혈관을 필요로 합니다. 이러한 장기 특이 혈관 전문화의 획득은 종종 장기 혈관화 과정과 분자적으로 관련이 없다고 여겨집니다. 여기서는 이 모델과 대립하여, 우리는 뇌 특이적 혈관형성을 위한 분자 메커니즘을 밝혀내었습니다. 이는 잘 알려진 blood–brain barrier maturation 신호인 Wnt7a/b ligand의 조절 하에 작동합니다.
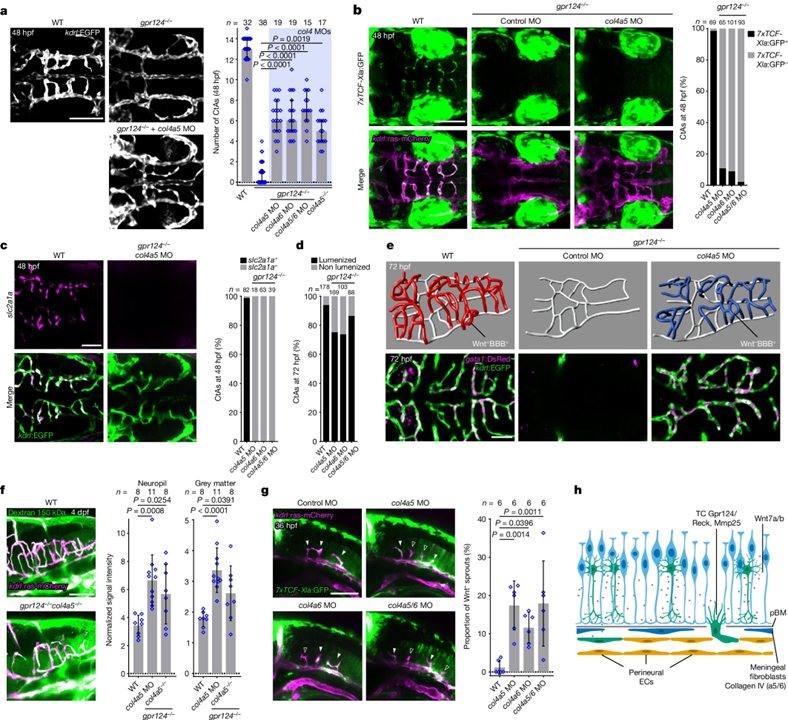
이 조절 메커니즘은 뇌 내피세포에서 풍부하게 발현되는 Mmp25에 의존합니다. Zebrafish 에서의 CRISPR-Cas9 mutagenesis를 통해, 이 미지의 당체 결합 표방인 matrix metalloproteinase가 뇌 표면을 덮는 뇌 복막 기저막을 횡단하는 tip cell에서 선택적으로 필요함을 밝혀냈습니다. Mmp25는 기계적으로, 중심 나선 부분의 짧은 비콜라겐 영역 내에서 뇌 침습 능력과 병적 진입 능력을 부여합니다. 병적 진입 능력은 매질 섬유아세포에서 유래하는 콜라겐 IV α5/6 사슬을 가위로 자르는 것에 의해 획득됩니다. 뇌 복막 구성에 유전적 간섭을 가한 후에는, 뇌혈관형성에 대한 Wnt-β-catenin 의존적인 장기형 조절이 손실되어 결과적으로 적절한 패턴화가 이루어지지만, blood–brain-barrier-defective가 있는 뇌혈관구조가 생성됩니다.
우리는 장기 특이적 혈관형성 메커니즘을 밝혀내고, tip cell의 메커니스트적 혈관다양성에 대한 새로운 시선을 제공하며, 이를 통해 장기가 혈관형성 tip cell에 지역적 제약을 부여함으로써 특징적인 생리적 요구를 충족시키는 혈관을 선택할 수 있다는 것을 보여줍니다.