Clathrin-associated AP-1은 STING 신호의 종료를 조절합니다.
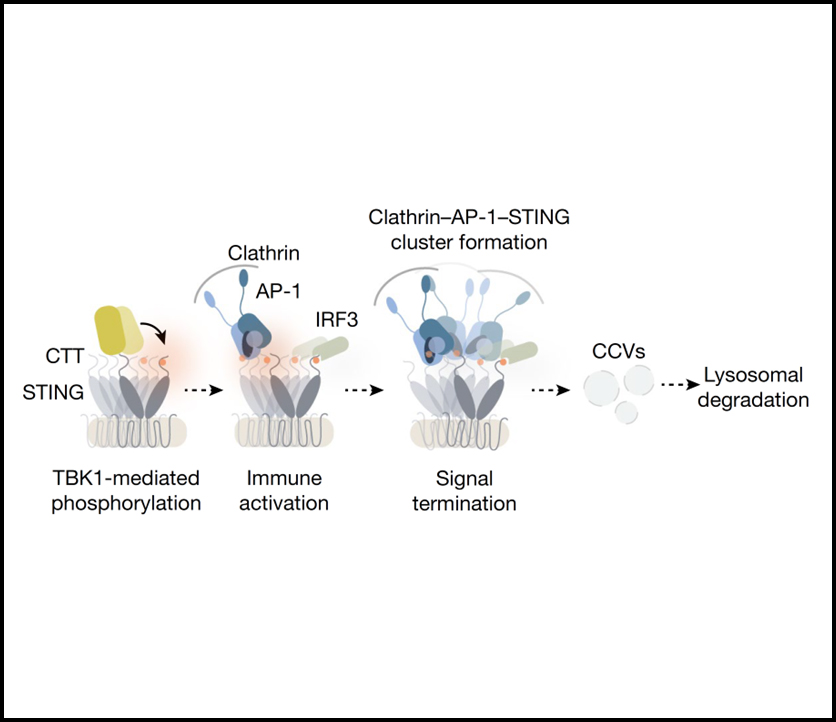
Abstract
Stimulator of interferon genes (STING)은 DNA sensing에서 cyclic GMP-AMP synthase의 downstream 기능을 하거나 감염, 암, 면역치료 동안 면역을 활성화하기 위해 bacterial cyclic dinucleotide와 small molecule에 대한 직접적인 수용체로 기능합니다. STING의 정확한 조절은 균형 잡힌 면역 반응을 보장하고 유해한 autoinflammation을 예방하는 데 필수적입니다. 활성화 후, 막 관통 단백질인 STING은 ER에서 golgi로 이동하며, 여기서 protein kinase TBK1에 의한 인산화는 신호 전달을 가능하게 합니다. Golgi에서 STING 신호를 종료하는 메커니즘은 아직 알려지지 않았습니다. 우리는 adaptor protein complex 1 (AP-1)이 STING-dependent immune activation의 종료를 제어한다는 것을 보여주었습니다. 우리는 AP-1이 인산화된 STING을 clathrin으로 코팅된 transport vesicle로 분류하여 STING이 분해되는 endolysosomal system으로 전달한다는 것을 발견했습니다. 우리는 STING의 cytosolic C-terminal tail (CTT)에서 highly conserved dileucine motif를 발견했고 그와 동시에 TBK1-dependent CTT phosphorylation도 발견하여 STING의 AP-1 참여를 지시하는 motif를 확인했습니다. 인산화된 STING과 complex를 이룬 AP-1의 저온 전자 현미경 구조는 TBK1-activated STING의 향상된 인식 과정을 설명합니다. 우리는 AP-1의 억제가 STING-induced immune response를 악화시킨다는 것을 보였습니다. 우리의 결과는 STING의 negative regulation의 구조적 메커니즘을 밝히고 신호의 개시와 종결이 면역의 일시적인 활성화를 가능하게 하는 것에 불가분의 관계가 있음을 확립합니다.
Figures
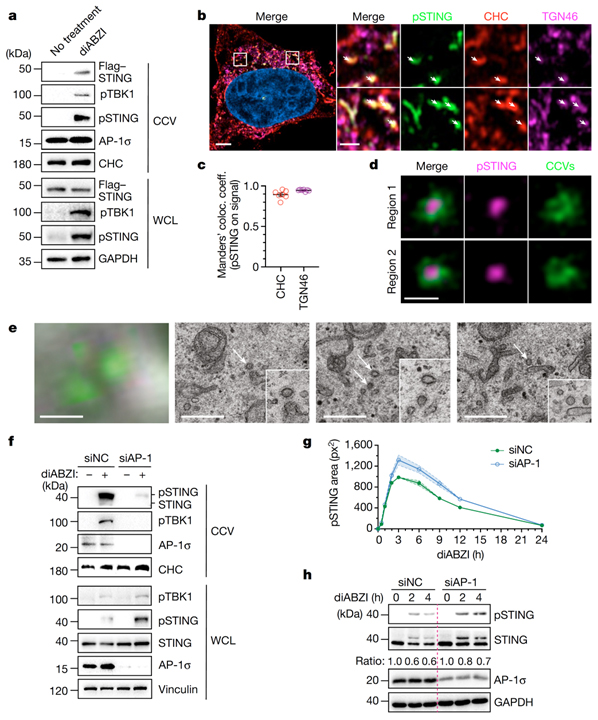
Fig 1. TGN에서 CCV (clathrin-coated transport vesicle)로 STING의 AP-1 로딩.
(A) Flag-tagged STING을 발현하는 HeLa 세포 (HeLa_STING)의 WCL과 CCV fraction에 대한 western blot 결과.
(B) diABZI로 자극된 HeLa_STING 세포의 Airyscan 이미지.
(C) (B)의 이미지를 Manders의 colocalization 계수를 사용하여 pSTING와 CHC (Clathrin heavy chain)의 colocalization 정량화.
(D) mCherry-clathrin과 Flag-STING으로 transfection 되고 diABZI로 자극된 세포에서 CCV에 둘러싸인 pSTING을 보여주는 STED 이미지.
(E) diABZI로 자극된 HeLa_GFP-STING 세포의 CLEM.
(F) siNC 또는 siAP-1을 처리하고 diABZI로 자극한 HeLa 세포의 WCL, CCV fraction에 대한 western blot 결과.
(G) siRNA로 처리되고 diABZI로 자극된 HeLa_STING 세포의 bright-field fluorescent microscope 이미지에서 pSTING 영역의 정량화.
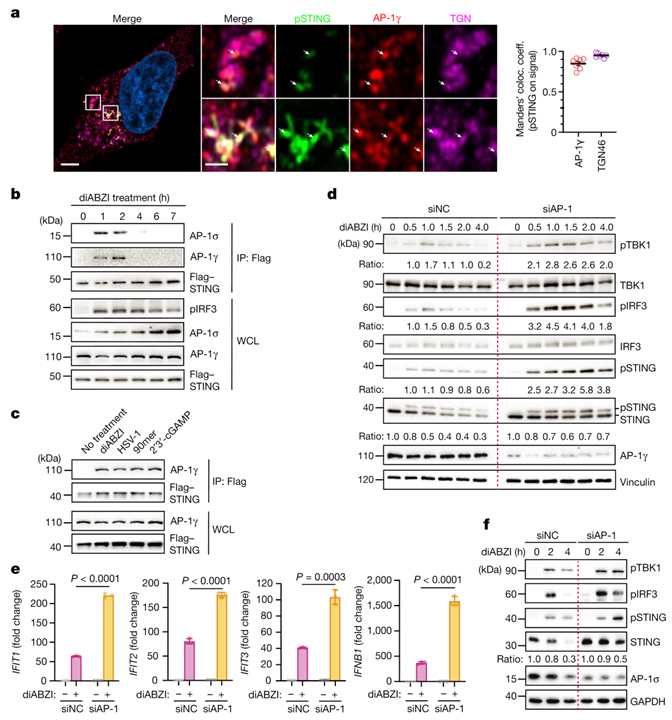
Fig 2. AP-1 binding의 STING degradation 지시로 인한 면역 활성화 제한.
(A) diABZI로 2.5시간 동안 자극된 HeLa_STING 세포의 Airyscan 이미지.
(B) HeLa_STING 세포를 diABZI로 자극 후 anti-Flag antibody로 Immunoprecipitation (IP)한 western blot 결과.
(C) HeLa_STING 세포를 2시간 동안 diABZI로 자극하고, 6시간 동안 HSV-1으로 감염시키거나 90mer dsDNA(1μg)로 3시간 또는 1μM 2’3′-cGAMP로 6시간 동안 transfection 시키고 anti-Flag antibody로 IP 후 western blot 결과.
(D) siRNA로 transfection 된 HeLa 세포를 diABZI로 자극하고 웨스턴 블롯으로 분석하였다. Vinculin을 로딩 컨트롤로 사용했습니다.
(E) siRNA로 transfection 되고 3시간 동안 diABZI로 처리된 HeLa 세포에서 IFNB1, IFIT1, IFIT2, IFIT3 발현의 유도에 대한 RT-qPCR 결과.
(F) 3일 동안 siRNA로 transfection 된 WI-38 human fibroblast를 diABZI로 자극한 western blot 결과.
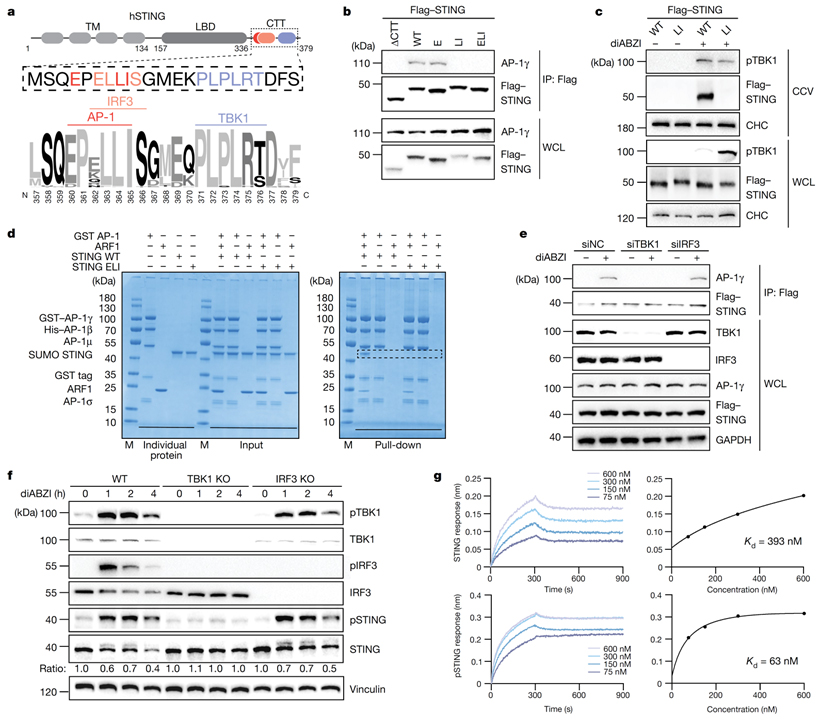
Fig 3. TBK1-dependent phosphorylation의 AP-1에 대한 STING binding 제어.
(A) 50종에서 표시된 인간 STING (hSTING)의 CTT와 CTT sequence logo의 개략도.
(B) Flag-tagged STING ΔCΤΤ (Δ1–341), WT STING, STIN GE(E360A), STING LI(L364A/I365A) 또는 STING ELI(E360A/L364A/I3)로 transfection 된 HeLa STING-KO 세포를 diABZI로 2시간 동안 처리 후 anti-Flag antibody로 IP한 western blot 결과.
(C) Flag-tagged WT STING 또는 STING LI로 reconstitute 되고 diABZI로 처리되거나 처리되지 않은 HeLa STING KO 세포에서 WCL과 CCV fraction에 대한 western blot 결과.
(D) ARF1이 있거나 없는 GST-tagged AP-1 core에 의한 WT LBD-STING 또는 LBD-STINGE LI의 GSH pull-down 결과.
(E) siNC 또는 TBK1, IRF3에 대한 siRNA로 transfection 된 HeLa_STING 세포에 diABZI 처리 후 anti-Flag antibody로 IP한 western blot 결과.
(F) 0, 1, 2, 4시간 동안 diABZI로 자극된 HeLa WT 세포, HeLa TBK1 KO 세포, HeLa IRF3 KO 세포의 western blot 결과.
(G) AP-1 ΔμCTD를 사용한 LBD-STING (상단) 또는 TBK1-phosphorylated LBD-STING (pSTING) (하단)의 bio-layer interferometry 결과.
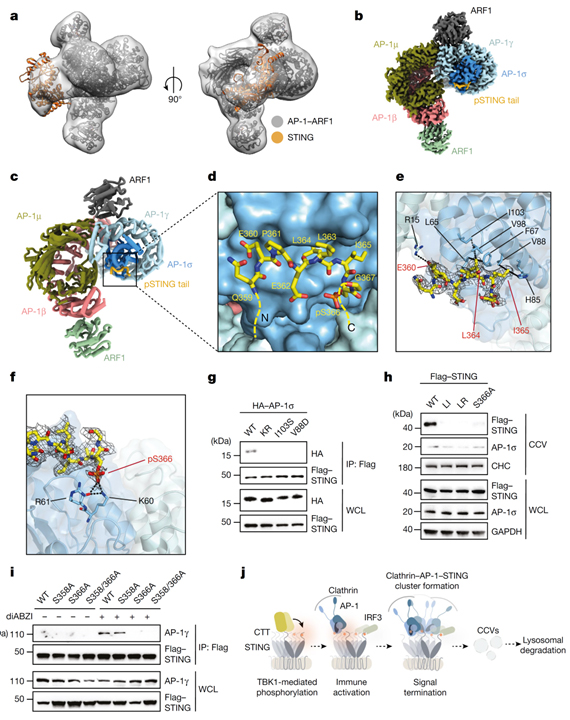
Fig 4. AP-1에 의한 STING recognation의 phospho-regulation을 위한 구조적 기초.
(A) 두 가지 다른 방향에서 complex의 3차원 (3D) 재구성 이미지.
(B) 3σ에서 윤곽을 그리는 2.34Å 분해능에서 AP-1 core와 pSTING tail에 대한 고해상도 3D 재구성 이미지.
(C) AP-1 pSTING complex 구조의 ribbon representation.
(D-F) Binding interface에 대한 상세 보기.
(E) 점선으로 표시된 EXXXLI motif 주변의 잠재적인 소수성 상호작용.
(F) 점선으로 표시된 pS366 주변의 잠재적 수소 결합.
(G) Flag-tagged STING, HA-tagged WT AP-1σ 또는 AP-1σ mutant σ KR(K60A/R61A), σ(I103S), σ(V88D)로 transfection 된 HEK293T 세포를 2시간 동안 diABZI로 자극 후 anti-Flag antibody로 IP한 western blot 결과.
(H) Flag-tagged WT STING과 STING mutant들: STING LI, STING LR(L374A/R375A), STING(S358A)으로 reconstitution된 diABZI 처리 HeLa STING KO 세포의 WCL, CCV fraction에 대한 western blot 결과.
(I) Flag-tagged STING과 STING mutant들: STING(S358A), STING(S366A), STING(S358/366A)으로 reconstitution된 HeLa STING KO 세포에 2시간 동안 diABZI로 처리 후 anti-Flag antibody로 IP한 western blot 결과.
(J) STING 신호 종료 시 AP-1 기능의 개략도.
Discussion
우리의 결과는 STING의 negative-feedback 제어의 기초가 되는 상세한 메커니즘에 대한 통찰력을 제공하고 이전 연구와 함께 STING-dependent immune response의 TGN-compartmentalized regulation 모델을 지원합니다. 첫째, STING oligomer는 TBK1에 결합하여 STING CTT의 강력한 인산화를 일으켜 downstream 요인과의 상호작용을 위한 플랫폼을 만듭니다. 신호의 활성화는 IRF3 recruitment, phosphorylation, nuclear translocation의 반복 주기에 의해 결정되는 반면 신호의 비활성화는 활성화된 STING을 nascent clathrin coat로 분류하는 것을 조절하는 AP-1 recognition에 의해 제어됩니다. 따라서 Golgi에서 신호 전달의 시작과 종료는 생화학적으로 결합되어 STING에 의해 유도된 면역 활성화를 자가 제한하는 분자적 메커니즘을 제공합니다.
우리의 구조 분석은 인산화에 의한 primary dileucine binding motif의 리모델링을 통해 AP-1이 STING의 활성화된 상태의 우선적 인식을 가능하게 하는 방법을 보여주었습니다. Coat 형성은 clathrin triskelion와 vesicle budding 촉진을 효율적으로 cross-bridge하기 위해 많은 수의 개별 ‘adapted’ cargo의 클러스터링에 의존하는 고도로 협력적인 프로세스입니다. 따라서 인산화에 의해 제공되는 분류 인터페이스에서 상대적으로 적당한 친화도 증가는 세포 수준에서 cargo selection에 영향을 미칠 수 있습니다. 특히, HIV-1M-Nef의 맥락에서 이전 연구는 단일 인산화가 AP-1에 의한 dileucine motif 및 tetherin의 하향 조절을 억제하는 기능을 할 수 있음을 보여주었습니다. 이것은 우리의 발견과 함께 할 때 상당한 수준의 적응성을 보여주며, 인산화는 dileucine binding을 개선하고 AP-1이 별개의 cargo state를 구별할 수 있도록 이용될 수 있습니다.
동물의 높은 보존성에도 불구하고 CTT는 척추동물의 STING에서만 등장하여 autophagy와 NF-κB 신호 전달을 포함한 primordial antiviral effector 기능을 보완하는 IFN-based immunity를 가능하게 합니다. 유사한 방식으로, 여기에서 설명하는 IFN-inducing STING의 제거로 이어져가는 AP-1-mediated trafficking process는 STING의 autophagy-mediated degradation을 보완합니다. STING CTT에서 AP-1 recruitment motif의 주목할 만한 conservation은 척추동물에서 type I IFN signaling module의 획득이 own integrated regulatory system과 함께 진화했을 수 있음을 시사합니다.
요약하면, TGN에서 negative-feedback의 메커니즘을 공개함으로써 우리의 연구는 STING-dependent immunity에 대한 보다 완전한 이해를 제공하고 therapeutic intervention을 위한 STING의 immunogenic effect를 조정하기 위한 개념적 전략을 제공할 수 있습니다.